
-

����ͨ��
����ץס�����Ƽ�
����������
���ڴ�ѧ����CRISPR/Cas���ڷ����к��¹ڲ�����RNA������
�����壺 �� �� С �� ʱ�䣺2023��05��26�� ��Դ�����ڴ�ѧ�����뺣���ѧѧԺ
�༭�Ƽ���
�������������壨aptamer����ŵ�������Jack Szostak����[1]����һ��̵ġ�����DNA��ssDNA����RNA�Ѻ�����
���������壨aptamer����ŵ�������Jack Szostak����[1]����һ��̵ġ�����DNA��ssDNA����RNA�Ѻ����ᣬͨ���γ���ά�ռ�ṹ������ض�������ϸ���������á���������ص�����ѧ�ͻ�ѧ���ԣ�����������������������Լ�������ҩ��Ŀ���[2]��ָ������������ϵͳ����������SELEX���Ǻ���������ɸѡ�Ľ����������Ҫ���ں����Ŀ���Ŀ�군��ϸ������Һ�л�����ϸ��������������ã��ٽ����Ȳ�������[3]�����ͬʱ����CRISPR/Cas�ĸ��죬�Ѿ���չ��ԶԶ��������Ȼ����ø�Ĺ��ܣ���չ����ת¼���ء������Ŵ����ء��������ǵȷḻ��ʵ�Ӧ��[4]��
2023��5��19�գ����ڴ�ѧ�����뺣���ѧѧԺ���������飬���Ϲ��ݹ���ʵ�����Խ�����ڣ��廪��ѧ̷���о�Ա���й���ѧԺ�����о����ܱ��о�Ա�Լ����ڼ����������������ڣ���Advanced Science��IF=17.5���Ϸ�������ĿΪRepurposing CRISPR/Cas to Discover SARS-CoV-2 Detecting and Neutralizing Aptamers������[5]��������һ����ӱ�Ļ���CRISPR/Cas��RNA����ɸѡϵͳ��CRISmers��CRISPR based aptamers screening system�����б��ڴ�ͳ��SELEXɸѡ��CRISmers��RNA������ɸѡ����Һ��ϵ����ϸ������ᵽ��ϸ���ڣ��Ӷ��ṩ�˰�����Ȼ���ﻷ���µ�RNA�͵����ʵ��۵�������ã���������ɸѡ�����еĻ�������Ӱ�졣CRISmersͨ��CRISPR/Cas��ת¼����ܣ���RNA��������е���������ת��Ϊ������ɸѡѹ����ϸ���Ĵ����������ÿ����ϸ����Ϊ������������Ԫ�����ֹ������¼��ͱ���������

���ȣ����Ŷ�������CRISmers�ĸ��Ȼ��Ӧ��GFP�ʹ�ǰ��SELEXɸѡ��õ�RNA����������˳����ĸ�����֤��ɸѡϵͳ�Ĺؼ�����ָ�����Ӷ��õ���CRISmersɸѡϵͳ�Ĺ������̡�����˵������������������Ŀ���pooled��ʽ�����sgRNA�Ǽܣ����Ŀ��к������ض��е���ϵ������У�������ļ��е����ںϵ�ת¼�������ӣ��Ӷ��������ο��Ի���ı��ͨ��ʩ�ӿ���ɸѡѹ�������ɽ�Я���������ϸ������ϵ�и���������RNA��������Ŀ�ͨ�����������ͣ����Ͻ���ϸ�������顣RNA�������������Ϣ����ͨ����ȡ�����顢���������������Ρ��Լ���Ȳ����ȡ��

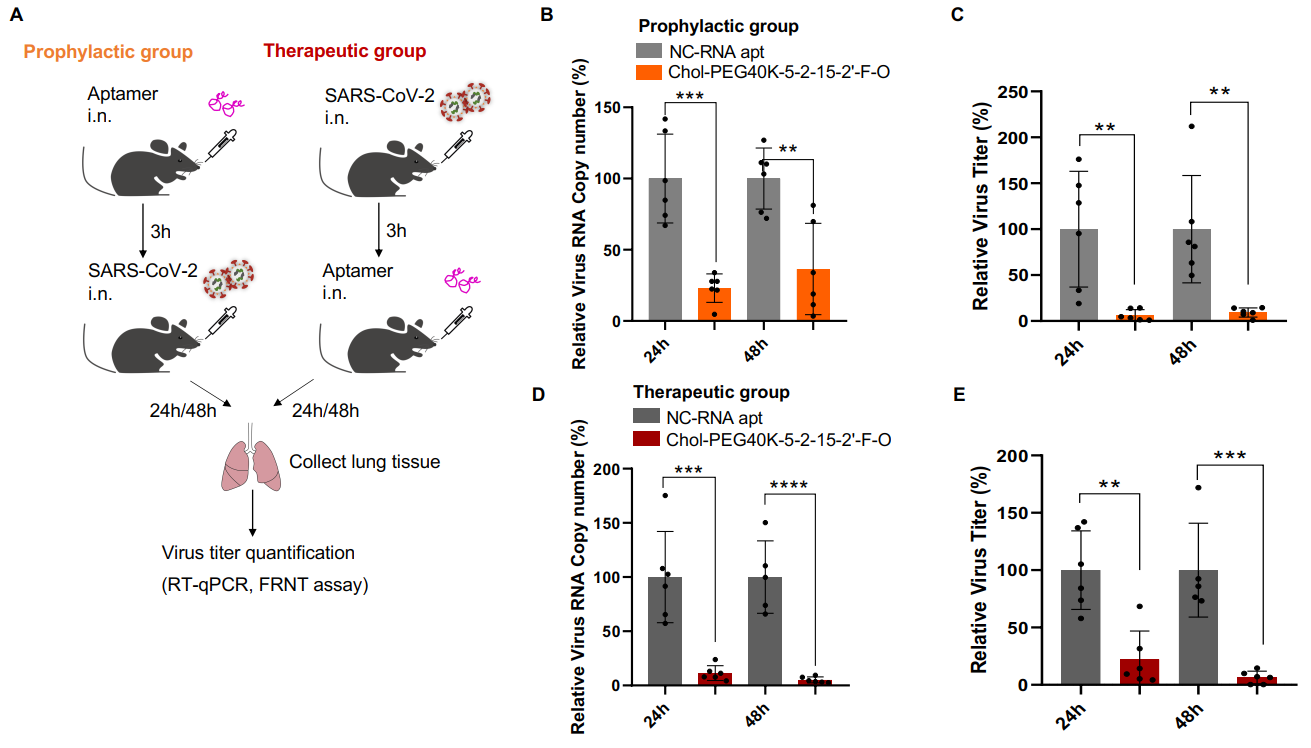
CRISmers�����Ͼ��й㷺�İ����ԣ������ǵ��о������ڼ���ֵ�¹����飬���Ŷӽ���һ���б�ָ����SARS-CoV-2��ͻ��������ṹ��RBD��ͨ������ɸѡ�Ͷ�����֤������˿��������RBD��2����ѡ��RNA�����壬����������ֳ���Ч�IJ��������кͻ��ԡ���Ȥ���ǣ������������б�����һ��[6]������������ֳ����ܲ���ͻ��Ӱ��������й���SARS-CoV-2��DZ������һ����Ҳ���ͺ����������ڵ����Խṹ�����йء����Ƶģ���ͬ��CRISPR/Casϵͳ����RNAҲ�۲쵽���Ի���������[7]����һ����ѡȡ����һ��RNA�����壬�Ŷӷ��֣���϶������κ�ż��������2��-����ऺ�2��-������RNA���Σ�����RNA�ȶ��ԣ����Լ�5���˵��̴����ʵݵ���������Ƥϸ�����棩�ͷ�����Ϊ40kDa�ľ��Ҷ������ӳ����ڰ�˥�ڣ���ż�������αǸ�ҩ����С������ʵ���˶�Omicron BA.2�����Ԥ���ͺ������Ϳ������кͻ��ԡ�ͨ���Ա�ʵ�飬�Ŷӷ��ֵ��̴��;��Ҷ�����ż�����ڶ������ڵĻ��Բ��ɻ�ȱ���������Ƕ���ϸ��ˮƽ�ϵ��кͻ��Կ��п��ޡ�
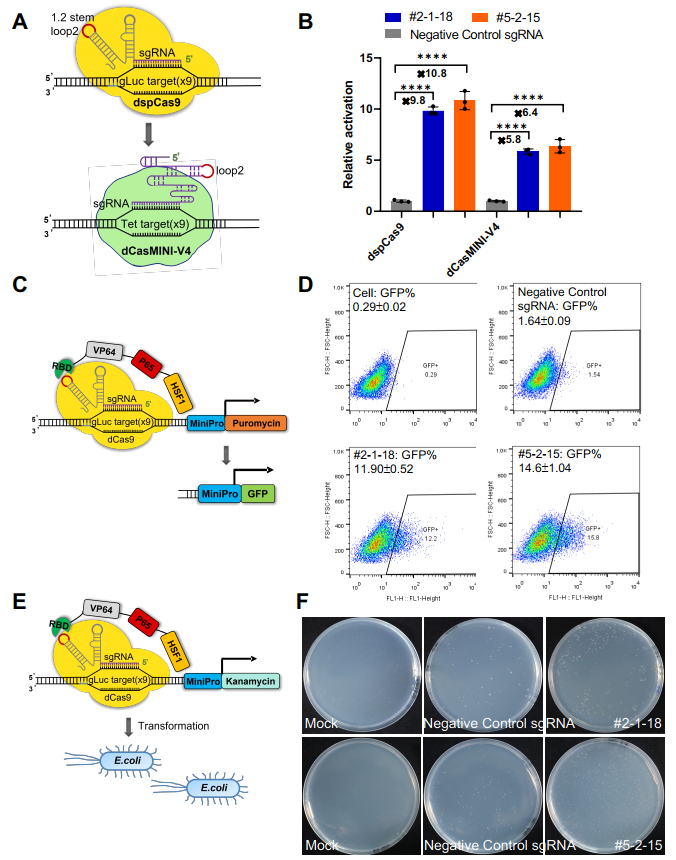
����Ŷӻ���CRISmersϵͳ��ͨ�������Խ�������֤��Ӧ�ð���SARS-CoV-2 RBDɸѡ��õ�����RNA���壬��CRISmersϵͳ�е�Ԫ���ֱ�������滻��������1����dSpCas9�滻�ɸ�С����汾��dCasMINI-V4[8-10]��2�������Ի����滻��ӫ�⵰�ף���3����ɸѡ����ϸ������HEK293Tϸ��ϵ�滻�ɴ˾������ɲ���RNA������RBD�������źš�
����������ҩ��ijɹ���Ҫ�������ԡ���Ϣ���ӡ��������õķ�ʽ������siRNA, ASO, mRNA����֮��Ӧ���ǣ�RNA��Ϊ���ṹ��������Ȼ��������ѧ�ĺܶ��Ҳ�dz���Ҫ��ij�������ϣ�CRISPR/Cas�е���RNA����һ����aptamer����[11]�������������Ľ�ɫת��Ϊҩ���ȻDZ�����д�����CRISmers��Ϊ�о�RNA��Ϊ���ṹ���ӡ��Ĺ����������ܷ���һ�������á����⣬CRISmers���ܿ�����Ҳ������Ĥ��İб꣬�����϶��Զ���Ĥ�ڵİб���и��Ӷ��صļ�ֵ��siRNA��mRNA�Ⱥ���ҩ����ϸ��Ĥ����ʵ�����ǵ��ٴ�Ӧ�þ�����Ҫ����[12]�����ź�����ͼ����Ľ��������ڰе���ں���ҩ�����Ҳ������ú�С���ӻ�ѧҩһ���Ŀɼ��ԡ���ˣ����ڸ����ĵĹ���������CRISmers�ĵ�һ���е㣬��λ�ڲ������棬��ɸѡϵͳ�д�����б����ʱ��ļ��顣���£����������ɹ����Ŷ������ƽ����¹ڲ����ĺ�ѡ����ҩ�������ٴ�Ӧ�õĿ������������µIJ�����ʾ�������б�������ѡRNA���������XBB.1.5��XBB.1.16�ٲ������ֻ��ԡ����ͬʱ�����������ʱ����CRISmers���ڱ����ڰ���֢�ȼ������о���
�й���ѧԺ�����о�����ʿ���žպ��ݹ���ʵ���Ҳ�ʿ���찮��Ϊ�����ĵĹ�ͬ��һ���ߣ�������ڡ��Խ����ڡ�̷���о�Ա���ܱ��о�Ա������������Ϊ�����Ĺ�ͬͨѶ���ߡ�
ԭ�����ӣ�
https://doi.org/10.1002/advs.202300656
�ο����ף�
1. Ellington, A.D. and J.W. Szostak, In vitro selection of RNA molecules that bind specific ligands. Nature, 1990. 346(6287): p. 818�C822.
2. Li, L., et al., Nucleic Acid Aptamers for Molecular Diagnostics and Therapeutics: Advances and Perspectives. Angewandte Chemie-International Edition, 2021. 60(5): p. 2221-2231.
3. Zhou, J.H. and J. Rossi, Aptamers as targeted therapeutics: current potential and challenges. Nature Reviews Drug Discovery, 2017. 16(6): p. 440.
4. Xu, X. and L. Qi, A CRISPR-dCas toolbox for genetic engineering and synthetic biology. Journal of Molecular Biology, 2019. 431(1): p. 34�C47.
5. Zhang, J., et al., Repurposing CRISPR/Cas to Discover SARS-CoV-2 Detecting and Neutralizing Aptamers. Adv Sci (Weinh), 2023: doi.org/10.1002/advs.202300656.
6. Sun, M., et al., Spherical neutralizing aptamer suppresses SARS-CoV-2 Omicron escape. Nano Today, 2022. 44: p. 101499.
7. Wei, J., et al., Closely related type II-C Cas9 orthologs recognize diverse PAMs. Elife, 2022. 11: p. e77825.
8. Xu, X., et al., Engineered miniature CRISPR-Cas system for mammalian genome regulation and editing. Molecular Cell, 2021. 81(20): p. 4333�C4345 e4.
9. Wu, Z., et al., Programmed genome editing by a miniature CRISPR-Cas12f nuclease. Nature Chemical Biology, 2021. 17(11): p. 1132�C1138.
10. Kim, D.Y., et al., Efficient CRISPR editing with a hypercompact Cas12f1 and engineered guide RNAs delivered by adeno-associated virus. Nat. Biotechnol., 2022. 40(1): p. 94�C102.
11. Wang, X.W., et al., RNA structure probing uncovers RNA structure-dependent biological functions. Nat Chem Biol, 2021. 17(7): p. 755-766.
12. Paunovska, K., D. Loughrey, and J.E. Dahlman, Drug delivery systems for RNA therapeutics. Nat Rev Genet, 2022. 23(5): p. 265-280.
 ����ͨ�Ź��ں�
����ͨ�Ź��ں�
���ѣ�CRISPR/Cas|�к��¹ڲ���|RNA������|
֪����ҵ��Ƹ