
-

生物通官微
陪你抓住生命科技
跳动的脉搏
纳米药物封装碳(nanoDECON)增强抗病毒疗效、生物利用度及胞内递送能力的研究
【字体: 大 中 小 】 时间:2025年10月02日 来源:Scientific Reports 3.9
编辑推荐:
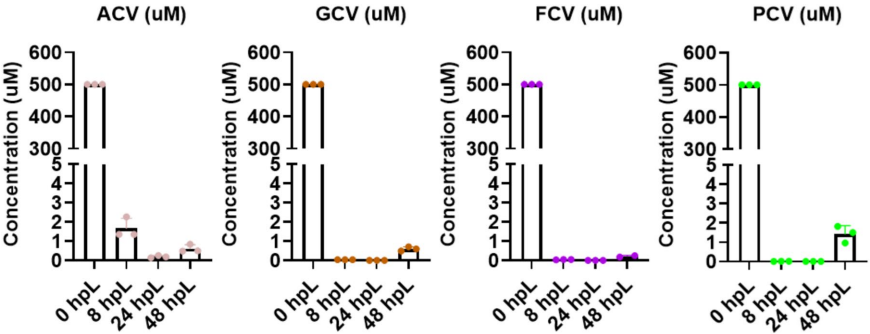
为解决单纯疱疹病毒1型(HSV-1)眼部感染治疗中药物生物利用度低、需频繁给药等问题,研究人员开发了基于纳米颗粒的药物封装碳(nanoDECON)递送系统。研究证实该系统可高效负载核苷类似物(如ACV、GCV、PCV),实现病毒触发式缓释,显著增强抗HSV-1活性并具备胞内及核内递送能力,为眼科抗病毒治疗提供了新策略。




 生物通微信公众号
生物通微信公众号
知名企业招聘