
-

生物通官微
陪你抓住生命科技
跳动的脉搏
综述:CD8 T细胞在ZIKV感染中的动态变化及免疫细胞迁移:对神经炎症和治疗的启示
【字体: 大 中 小 】 时间:2025年07月16日 来源:Virology Journal 4
编辑推荐:
这篇综述深入探讨了CD8 T细胞在寨卡病毒(ZIKV)感染中的双重作用:既通过细胞毒性(perforin-granzyme通路)和细胞因子(IFN-γ/TNF-α)分泌发挥抗病毒保护,又可能通过血脑屏障(BBB)浸润引发神经炎症。文章系统分析了趋化因子(CCL2/CXCL10)介导的免疫细胞迁移机制,并探讨了S1P受体调节剂FTY720等治疗策略在平衡免疫保护与神经病理损伤中的应用前景。
CD8 T细胞:抗病毒防御的核心战士
作为适应性免疫的关键效应细胞,CD8+ T细胞(又称细胞毒性T淋巴细胞,CTL)通过MHC I类分子识别病毒抗原后,分化为具有杀伤能力的效应细胞。其清除感染细胞的机制主要包括:穿孔素-颗粒酶(perforin-granzyme)途径诱导靶细胞凋亡、FasL-Fas死亡受体通路,以及分泌IFN-γ和TNF-α等抗病毒细胞因子。在ZIKV感染模型中,特异性CD8+ T细胞能显著降低脑组织病毒载量,而CD8+ T细胞缺失则导致病毒复制失控和死亡率升高。
神经侵袭:免疫细胞的"特洛伊木马"策略
传统认为中枢神经系统(CNS)具有免疫特权,但神经嗜性病毒如ZIKV、西尼罗河病毒(WNV)能通过破坏血脑屏障(BBB)的紧密连接蛋白(如claudin-5),或借助感染单核细胞的"特洛伊木马"机制入侵。ZIKV感染的CD169+单核细胞通过CCR7/RAGE受体介导穿过BBB,将病毒递送至神经组织。星形胶质细胞和神经元产生的趋化因子(如CXCL10和CCL5)形成浓度梯度,引导表达CXCR3/CCR5的CD8+ T细胞向感染部位迁移。

双刃剑:保护与病理的微妙平衡
在ZIKV感染中,CD8+ T细胞展现出明显的双重性:一方面通过清除感染细胞限制病毒扩散,另一方面其过度激活可能导致神经损伤。小鼠模型显示,脑浸润的CD8+ T细胞虽能控制CNS病毒复制,但伴随出现的NKG2D+旁观者T细胞会引发神经元损伤和运动功能障碍。类似地,在睾丸组织中,CD8+ T细胞在清除病毒的同时可能引发睾丸炎。这种保护与病理的平衡在妊娠期尤为关键,过强的T细胞反应可能加剧胎儿神经发育异常。
治疗策略:精准免疫调控
针对ZIKV的治疗开发聚焦于三个方向:
疫苗(如DNA疫苗GLS-5700)通过诱导NS3蛋白特异性CD8+ T细胞建立长效保护;
抗病毒药物(如sofosbuvir)直接抑制病毒RNA聚合酶(NS5蛋白);
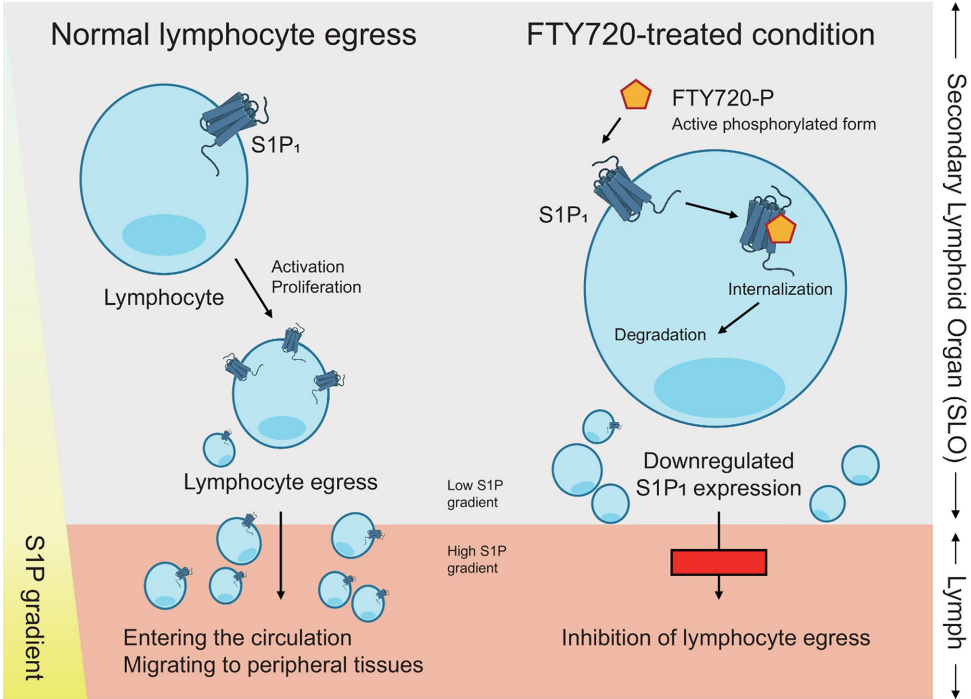
免疫调节剂FTY720通过S1P1受体调控淋巴细胞外渗,减少CNS炎症浸润。值得注意的是,恢复期血清中的中和抗体能穿越胎盘,在动物模型中显示出预防胎儿小头畸形的潜力。
未来展望:走向精准免疫干预
对CD8+ T细胞在神经嗜性病毒感染中时空动态的深入解析,将有助于开发既能维持抗病毒效力又可避免免疫病理的精准疗法。特别是针对TRM(组织驻留记忆T细胞)亚群的调控,以及CCR2/CXCR3趋化因子通路的靶向干预,可能为ZIKV相关神经并发症提供新的治疗窗口。跨物种研究显示,登革病毒(DENV)预感染诱导的交叉反应性CD8+ T细胞对ZIKV具有部分保护作用,这为流行区的疫苗设计提供了重要线索。
 生物通微信公众号
生物通微信公众号
知名企业招聘