
-

生物通官微
陪你抓住生命科技
跳动的脉搏
三重吸入疗法下COPD急性加重的分子机制:呼气代谢组学揭示氨基糖代谢紊乱与潜在治疗靶点
【字体: 大 中 小 】 时间:2025年09月28日 来源:Respiratory Research 5
编辑推荐:
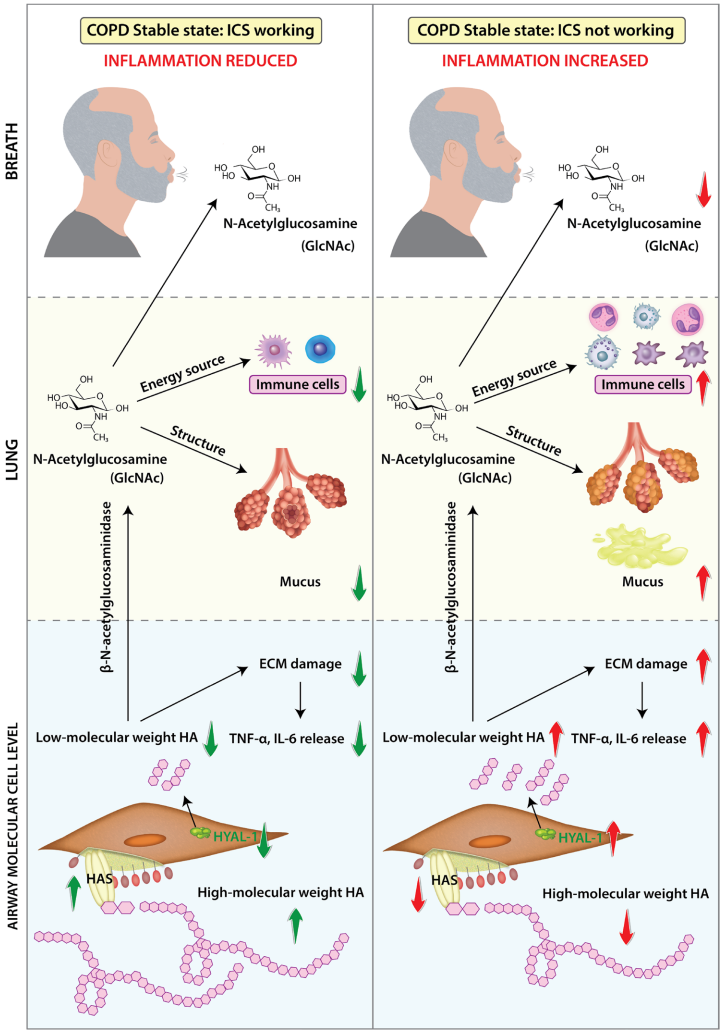
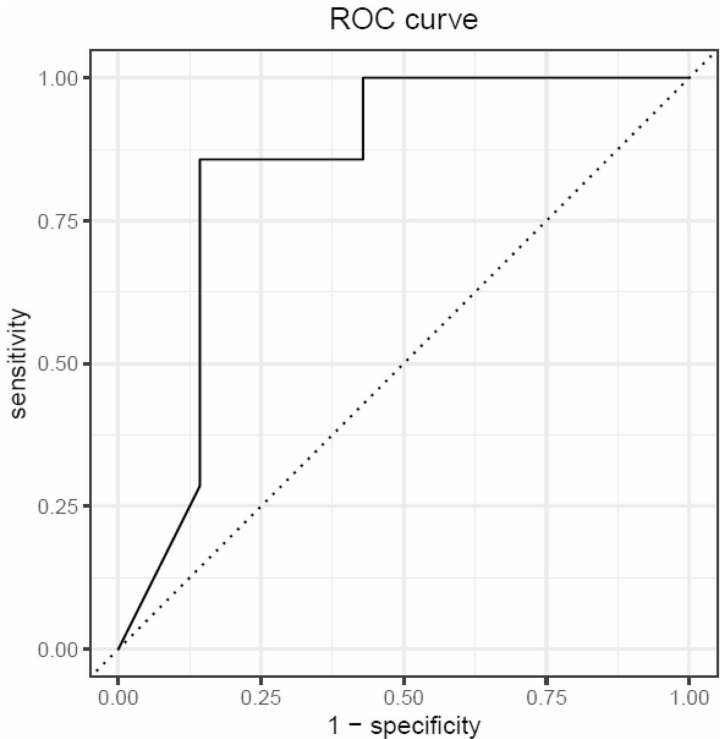
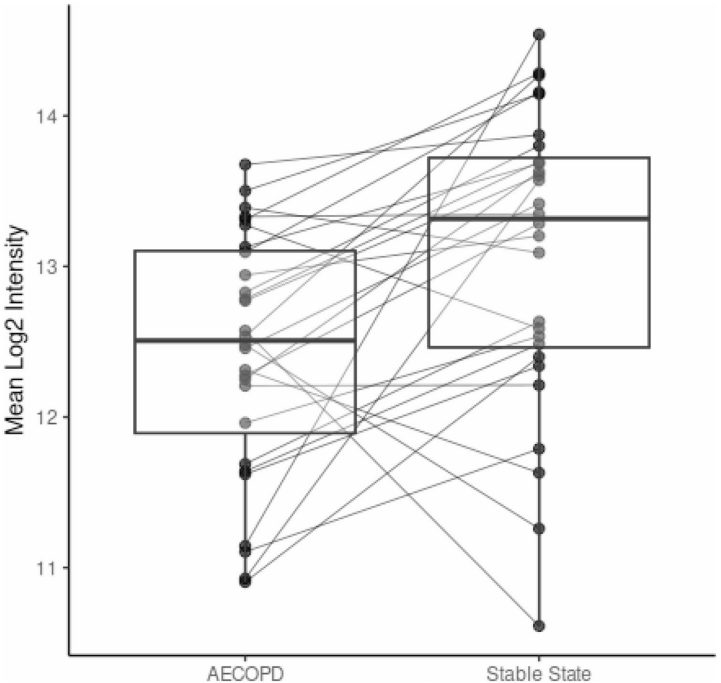
本研究针对接受三重吸入疗法(ICS/LABA/LAMA)仍发生急性加重(AECOPD)的COPD患者,通过实时二次电喷雾电离高分辨质谱(SESI-HRMS)分析呼气分子图谱。研究发现AECOPD期间氨基糖代谢(尤其是N-乙酰葡糖胺)、亚油酸和丁酸代谢通路发生显著改变,并构建出区分AECOPD与稳定状态的预测模型(AUC=0.84)。该研究为三重疗法应答不佳的COPD患者提供了潜在治疗靶点,且呼气分析技术有望实现AECOPD的快速诊断。
 生物通微信公众号
生物通微信公众号
知名企业招聘